 发病机制
发病机制
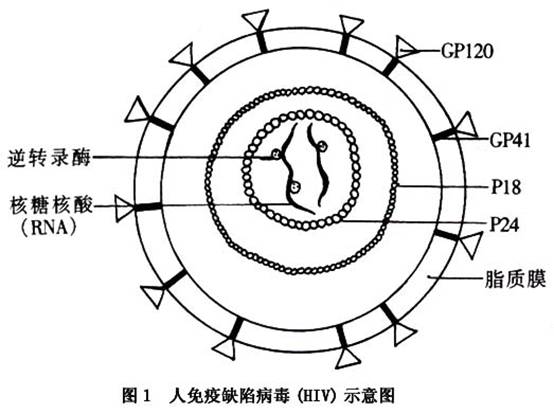
发病机制:HIV只能在宿主的活细胞内复制,HIV包含着遗传基因,但必须依赖宿主细胞才能产生新的病毒颗粒。病毒的遗传指令可嵌于核糖核酸染色体组(RNA病毒)或脱氧核糖核酸(DNA)染色体组(DNA病毒)。HIV是RNA病毒,它具有特殊的反转录酶,可使这种病毒将它的RNA复制成DNA,复制的DNA与感染的宿主细胞染色体组结合,病毒的蛋白与核酸构建为成熟的病毒体,通过芽生的方式被宿主细胞释放出来,从而完成病毒的复制。在正常状态下,是由DNA复制RNA的。由于HIV在复制过程中采取了相反的步骤,所以称为反转录病毒(图1)。
HIV外壳上的糖蛋白GP120与一些人细胞,如CD4 T淋巴细胞,巨噬细胞和神经系统的一些细胞表面的抗原分子(称为CD4或T4受体)具有特殊的亲和力。HIV感染可以损伤或杀死T4辅助性细胞,导致T辅助性细胞和T抑制性细胞比例逆转。正常健康人中,T辅助性细胞和T抑制性细胞的比例为1.0~2.0,但在艾滋病人中,这两者的比例降为1.0以下。这种T辅助性细胞和T抑制性细胞比例逆转导致了细胞免疫功能不全,从而引起机会性病原体引起的感染和不常见的肿瘤发生(图2)。
 临床表现
临床表现
临床表现:感染后潜伏期长短不一,短则1年,长则数年甚至10多年(平均4.5年)。全身有持续性发热、盗汗、
腹泻、消瘦、淋巴结肿大,T
H细胞减少,T
H细胞与T
S细胞比值倒置。由于细胞免疫功能低下,患者对无害的条件致病微生物呈高度易感性,发生多脏器、多系统感染并伴发恶性肿瘤。
据文献报道,AIDS有40%~92.3%并发眼部病变,其中眼底损害更为多见。
眼底损害,可发生于HIV感染本身,亦可发生于条件致病微生物的继发感染。
由HIV感染本身所致者主要表现为棉绒状斑,大多位于眼底后部血管弓附近或视盘周围的视网膜浅层,1个或多个,悄然出现,在4~6周内自行消失,继而在不同部位再发生新病灶。棉绒状斑为视网膜毛细血管前动脉炎症性阻塞,引起神经纤维层局灶性缺血、缺氧、轴浆流阻滞,神经纤维水肿变性而形成。F
FA在
白斑相应处(包括已消失处)为无灌注区(filling defect)。有时还可见到眼底后极部火焰状出血及有白色中心的出血斑。黄斑中心凹周围毛细血管闭塞,亦可导致黄斑水肿渗出,出现沿Henle纤维排列的放射状微囊样皱褶和星芒状斑。
HIV侵犯破坏免疫系统的核心TH细胞,形成不可逆转的免疫缺陷,从而引起各种条件致病微生物(病毒、细菌、真菌、原虫)感染性眼底疾病。如巨细胞病毒性视网膜炎、弓形虫性视网膜脉络膜炎、真菌(念珠菌、隐球菌等)性脉络膜视网膜炎、鸟型分枝杆菌性脉络膜视网膜炎等。
巨细胞病毒性视网膜炎(cytomegalovirus retinitis)在AIDS患者中发病率高达12%~46%(此外见于恶性肿瘤及脏器移植后应用免疫抑制药的患者)。通常见于病程晚期,但也可先于全身其他病变出现之前。开始时,进展缓慢,对中心视力无明显损害,患者往往并无感觉,或仅有飞蚊症。检眼镜下见到周边眼底或后极部血管弓附近有境界模糊、黄白色散在的颗粒状或灰白色絮样混浊,逐渐扩大融合。视网膜广泛性水肿、渗出及火焰状出血,黄斑星芒状斑,使眼底呈碎乳酪与番茄酱样。
弓形虫视网膜脉络膜炎(toxoplasmic retinochoroiditis)是因弓体原虫经后短睫状动脉进入脉络膜视网膜,或自脑脊液而到达视盘附近。眼底表现与一般后天性弓形虫性脉络膜视网膜炎相同。但炎症反应急剧,常因房水、玻璃体混浊而不能满意透见眼底。



 流行病学
流行病学
 病因
病因
 发病机制
发病机制

 临床表现
临床表现
 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查

 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后
 预防
预防